GLI IDRURI
Gli idruri sono composti binari, formati cioè da due elementi di cui uno è l'idrogeno.
In essi, se l'altro elemento appartiene ai gruppi 1 o 2 della tavola periodica (metalli alcalini o metalli alcalino - terrosi) l'idrogeno ha numero di ossidazione pari a -1 è l'idruro ha legami ionici.
Se l'altro elemento, al contrario, non appartiene ai gruppi 1 o 2 allora l'idrogeno ha numero di ossidazione pari a +1 e l'idruro ha legami covalenti.
In ogni caso, nella formula bruta l'idrogeno va scritto sempre per secondo.
ESEMPI DI IDRURI IONICI
- LiH = idruro di litio
- NaH = idruro di sodio
- CaH2 = diidruro di calcio
ESEMPI DI IDRURI COVALENTI
- CH4 = tetraidruro di carbonio (metano)
- NH3 = triirduro di azoto (ammoniaca)
- SiH4 = tetraidruro di silicio (silano)
- PH3 = triidruro di fosforo (fosfina)
GLI IDRACIDI
Gli idracidi sono composti binari, formati cioè da due elementi, in cui uno dei due è l'idrogeno e l'altro appartiene ai gruppi 16 e 17 della tavola periodica (tranne l'ossigeno).
In essi, l'idrogeno ha numero di ossidazione pari sempre a +1 e nella formula bruta va scritto per primo.
ESEMPI DI IDRACIDI
- HCl = cloruro di idrogeno (acido cloridrico)
- HBr = bromuro di idrogeno (acido bromidrico)
- H2S = solfuro di diidrogeno (acido solfidrico)
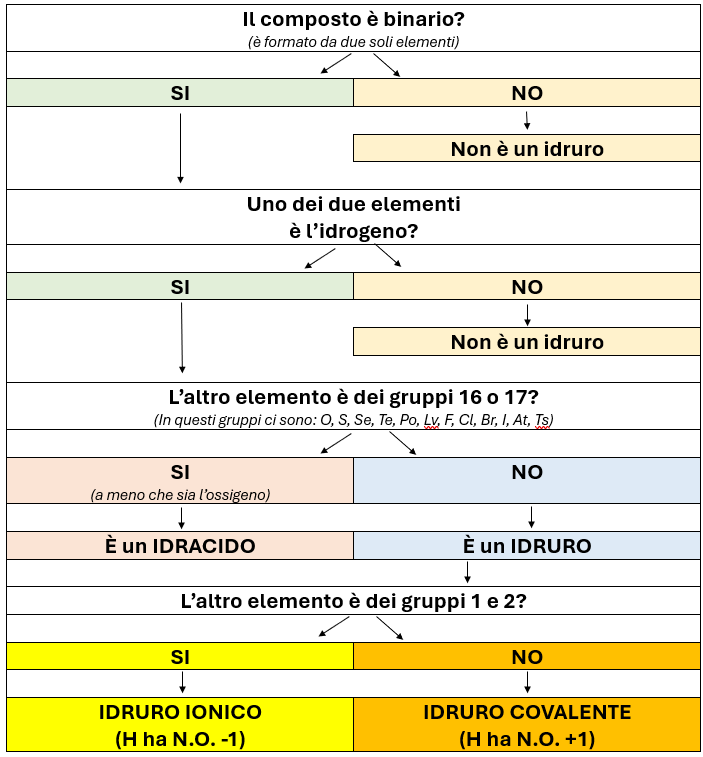
SCHEMA PER IL RICONOSCIMENTO
Infine, ecco un facile schema per la classificazione di idruri e idracidi
(richieste e confronti a riccardo@riccardoviselli.it; instagram.com/ricviselli/)