DEFINIZIONE
Gli ossidi sono composti binari, formati cioè da due elementi di cui uno è l'ossigeno.
In essi, l'ossigeno ha sempre numero di ossidazione pari a -2: sono pertanto necessari 2 elettroni per completare il suo ottetto.
L'altro elemento può essere:
- un metallo = formazione di ossidi basici
- un non metallo = formazione di ossidi acidi o anidridi.
ESEMPI DI OSSIDI BASICI
- Li2O = ossido di dilitio
- Na2O = ossido di disodio
- FeO = ossido di ferro (ossido ferroso)
- Fe2O3 = triossido di diferro (ossido ferrico)
ESEMPI DI OSSIDI ACIDI O ANIDRIDI
- CO = ossido di carbonio (anidride carboniosa)
- CO2 = diossido di carbonio (anidride carbonica)
- Cl2O = ossido di dicloro (anidride ipoclorosa)
- Cl2O3 = triossido di dicloro (anidride clorosa)
- Cl2O5 = pentossido di dicloro (anidride clorica)
- Cl2O7 = eptossido di dicloro (anidride perclorica)
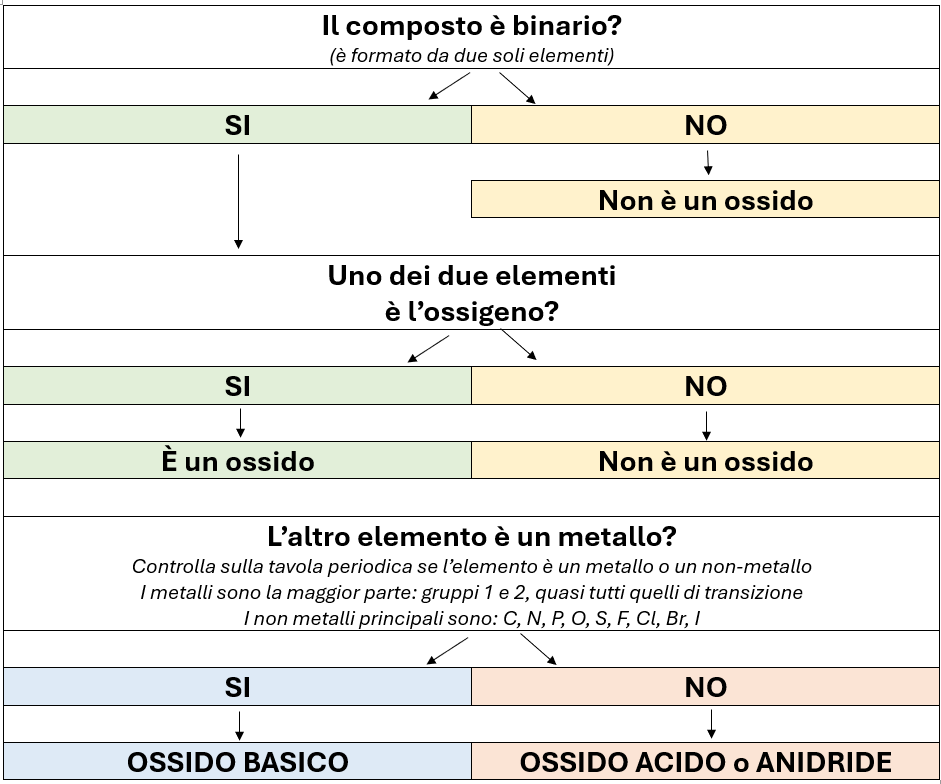
SCHEMA DI RICONOSCIMENTO DEGLI OSSIDI
Infine, ecco un pratico schema per il riconoscimento degli ossidi
(chiarimenti possono essere richiesti a riccardo@riccardoviselli.it; instagram.com/ricviselli/)